Page 166 - 南京医科大学学报自然科学版
P. 166
第41卷第7期
·1096 · 南 京 医 科 大 学 学 报 2021年7月
[3]
体开发抗体主要靶标。 相同,SARS⁃CoV⁃2也没有血凝素⁃酯酶(HE)基因 。
冠状病毒的 S 蛋白是高度糖基化的糖蛋白,相
对分子质量约 2×10 ,由 1 200~1 500 个氨基酸残基
5
组成。尽管4个种类冠状病毒的S蛋白氨基酸序列
膜蛋白 不同,但在结构上却具有一些共同特征:皆由较长
包膜蛋白
的膜外区、跨膜区和膜内区组成,属Ⅰ类病毒融合
[4]
RNA 蛋白 。像其他Ⅰ类病毒融合蛋白一样,S蛋白在翻
刺突蛋白 译后会折叠成亚稳态的预融合构象。运用冷电镜
核衣壳蛋白 (Cryo⁃EM)对SARS⁃CoV⁃2的S蛋白研究后发现,S蛋
[5]
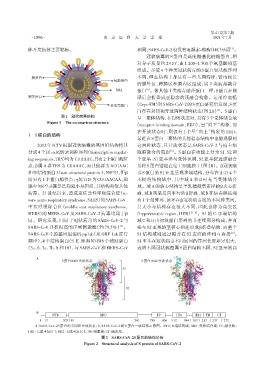
白存在封闭和开放两种结构状态(图2A) 。S蛋白
图1 冠状病毒结构 呈三聚体结构,在封闭状态时,具有3个受体结合域
Figure 1 The coronavirus structure
(receptor⁃binding domain,RBD),呈“向下”构象,而
在开放状态时,则仅有 1 个呈“向上”构象的 RBD。
1 S蛋白的结构
最近在S蛋白三聚体的其他稳态结构中也能观察到
2012 年 ICTV 根据冠状病毒的基因组结构将其 这两种状态,且开放状态是 SARS⁃CoV⁃2 与宿主细
[6]
分成4个属:α属转录调控序列(transcription regulat⁃ 胞膜融合的前提 。S 蛋白在功能上分为 S1、S2 两
ing sequences,TRS)均为 CUAAAC,具有2个蛋白酶位 个亚基:S1 亚基参与受体识别,S2 亚基促进膜融合
点;β属A群TRS为 CUAAAC,而其他群为ACGAAC 并将S蛋白锚定在宿主细胞膜上(图2B)。β冠状病
和非结构蛋白3(non⁃structural protein 3,NSP3),但β 毒 S 蛋白的 S1 亚基呈现多域结构,分布在 A~D 4 个
属只有1个蛋白酶位点;γ属TRS为CUUAACAA,都 不同的结构域中,其中域 A 和 B 可充当受体结合
缺少NSP7;δ属是已知最小基因组,其结构类似其他 域。域A的核心结构呈半乳糖凝集素样的β夹心折
病毒。21 世纪以来,造成重症急性呼吸综合征(se⁃ 叠,域 B 则呈反向平行的β折叠,域 B 在病毒膜远端
vere acute respiratory syndrome,SARS)的SARS⁃CoV、 有 1 个延伸环,该环在β冠状病毒属的不同种类间,
中东呼吸综合征(middle east respiratory syndrome, 其大小与结构存在很大不同,因此也称为高变区
[7-8]
MERS)的 MERS⁃CoV 及 SARS⁃CoV⁃2 病毒均属于β (hypervariable region,HVR) 。S1 的 C⁃末端结构
属。研究发现,同属于冠状病毒的 SARS⁃CoV⁃2 与 域 C 和 D 由初级蛋白序列的非连续部分构成,并直
SARS⁃CoV 具有很高的序列同源性(约 79.5%) 。 接与 S2 亚基的茎核心相连形成β折叠结构,而整个
[2]
[9]
SARS⁃CoV⁃2 的基因组编码 pp1ab(从 ORF 1ab 进行 S1 结构域则通过覆盖在 S2 表面的环相互连接 。
翻译),4 个结构蛋白(S、E、M 和 N)和 6 个辅助蛋白 S1亚基在冠状病毒不同属间的序列长度差异很大,
(3a、6、7a、7b、8 和 10),与 SARS⁃CoV 和 MERS⁃CoV 表明不同冠状病毒属 S 蛋白结构不同,S2 亚基则高
A
S蛋白RBD关闭状态 S蛋白RBD开放状态
S1
S2
B
NTD RBD FP HR1 HR2 TM CT
1 13 305 319 541 788 806 912 984 1 163 1 213 1 237 1 273
A:SARS⁃CoV⁃2S 蛋白的关闭和开放状态;B:SARS⁃CoV⁃2 刺突蛋白一级结构示意图。NTD:N 端结构域;RBD:受体结合域;FP:融合肽;
HR1:七肽重复区1;HR2:七肽重复区2;TM:跨膜域;CT:胞质尾。
图2 SARS⁃CoV⁃2S蛋白的结构分析
Figure 2 Structural analysis of S protein of SARS⁃CoV⁃2