Page 16 - 南京医科大学学报自然科学版
P. 16
第41卷第4期
·486 · 南 京 医 科 大 学 学 报 2021年4月
壁,剪碎消化后于无血清培养基中培养。7 d左右大
多数组织细胞死亡,NSC 可存活并分裂成团形成
NSC球(图1A)。在无血清培养基中,NSC呈悬浮状
态;在多聚赖氨酸和层黏连蛋白处理的培养皿中,
NSC变为单层贴壁细胞(图1B)。
2.2 CRISPR/Cas9敲除位点选择和打把载体构建
使用sgRNA在线设计软件,针对PIN1 的第2个
外显子设计 sgRNA(图 2A)。将 sgRNA 与 PX330 载 A B
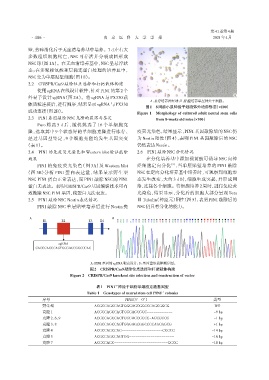
A:悬浮培养神经球;B:贴壁培养单层神经干细胞。
体质粒连接后,进行测序,结果显示sgRNA与PX330
图1 8周龄小鼠神经干细胞体外培养形态(×100)
成功连接(图2B)。 Figure 1 Morphology of cultured adult neural stem cells
2.3 PIN1基因敲除NSC克隆的获得与鉴定 from 8⁃weeks old mice(×100)
Puro 筛选 5 d 后,随机挑选了 16 个单细胞克
隆,选取其中 9 个状态好的单细胞克隆进行冻存, 疫荧光染色,结果显示,PIN1 基因敲除后的 NSC 仍
经过基因型鉴定,9 个细胞克隆均发生基因突变 为 Nestin 阳性(图 4),表明 PIN1 基因敲除后的 NSC
(表 1)。 仍然表达Nestin。
2.4 PIN1的免疫荧光染色和Western blot验证敲除 2.6 PIN1敲除NSC分化情况
效果 在分化培养基中添加视黄酸可诱导 NSC 向神
[9]
PIN1 的免疫荧光染色(图 3A)及 Western blot 经细胞定向分化 ,当单层贴壁培养的 PIN1 敲除
(图 3B)分析 PIN1 蛋白表达量,结果显示野生型 NSC 在定向分化培养基中培养时,可观察到细胞形
NSC PIN1 蛋白正常表达,而 PIN1 敲除 NSC 的 PIN1 态发生改变,大约 3 d 时,细胞生成突起,并形成网
蛋白无表达。表明CRISPR/Cas9基因编辑技术可有 络,连接各个细胞。待细胞培养2周时,进行免疫荧
效敲除NSC PIN1基因,使蛋白无法表达。 光染色,结果显示,分化后的细胞大部分呈现 Beta
2.5 PIN1敲除NSC Nestin表达情况 Ⅲ Tubulin(神经元)阳性(图5),表明PIN1敲除后的
PIN1 敲除 NSC 单层贴壁培养后进行 Nestin 免 NSC仍具有分化的能力。
A B
E1 E2 E3 E4
sgRNA
CACCGAGCCAGTGGGAGCGGCCCAG
A:PIN1基因的sgRNA靶点设计;B:基因重组载体测序图。
图2 CRISPR/Cas9敲除位点选择和打把载体构建
Figure 2 CRISPR/Cas9 knockout site selection and construction of vector
表1 PIN1 神经干细胞单细胞克隆基因型
-/-
Table 1 Genotypes of neural stem cell PIN1 colonies
-/-
序号 PIN1(5′→3′) 类型
野生型 ACGCCAGCCAGTGGGAGCGGCCCAGCGGCG WT
克隆1 ACGCCAGCCAGTGGGAGCGGC------------ -9 bp
克隆2、6、9 ACGCCAGCCAGTGGGAGCGGCC-AGCGGCG -1 bp
克隆3、8 ACGCCAGCCAGTGGGAGCGGCCCCAGCGGCG +1 bp
克隆4 ACGCCAGCCAG-------------------CGGCG -14 bp
克隆5 ACGCCAGCCAGTGG--------------------- -16 bp
克隆7 ACGCCAGC-------------------------GGCG -18 bp