Page 49 - 南京医科大学学报自然科学版
P. 49
第41卷第4期 侍崇龙,董洪权,金文杰. α⁃FMH抑制小胶质细胞的活化改善大鼠相关炎症与认知功能障碍[J].
2021年4月 南京医科大学学报(自然科学版),2021,41(04):516-521 ·519 ·
A Control α⁃FMH 了逃避恐惧实验评估大鼠的认知功能。结果如图4
所示,与Control组相比,LPS组大鼠出现了明显的恐
惧记忆损伤,僵立行为的时间明显缩短。而与LPS组
相比,α⁃FMH+LPS组大鼠僵立行为的时间明显增加,
说明α⁃FMH可缓解LPS诱导的大鼠认知功能下降。
LPS α⁃FMH+LPS
100
( % ) 80 #
60
B 僵立时间 40 *
80 ** 20
Iba1阳性细胞数/ 高倍视野 60 *# 与Control组相比,P < 0.01;与LPS组相比,P < 0.01(n=8)。
0
Control
α⁃FMH
α⁃FMH+LPS
LPS
40
#
*
20
图4 α⁃FMH可缓解LPS诱导的大鼠恐惧记忆损伤
0 Figure 4 α⁃FMH alleviates LPS⁃induced fear memory im⁃
Control α⁃FMH LPS α⁃FMH+LPS
pairment in rats
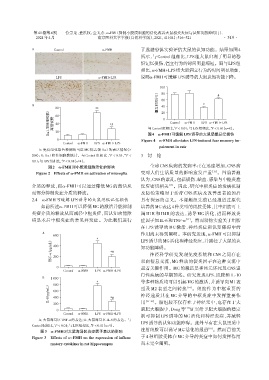
A:免疫组化染色检测海马区 MG 标志物 Iba1 的表达情况(×
*
**
200);B:Iba1 阳性细胞数统计。与 Control 组相比,P < 0.05,P < 3 讨 论
0.01;与LPS组相比,P < 0.01(n=4)。
#
图2 α⁃FMH对小胶质细胞活化的影响 全球 CNS 疾病的发病率正在迅速增加,CNS 病
Figure 2 Effects of α⁃FMH on activation of microglia 变对人们生活质量的影响愈发严重 [12] 。目前普遍
认为,CNS的紊乱,包括损伤、缺血、感染与中枢炎性
介质的释放,而α⁃FMH 可以通过降低 MG 的激活从 反应密切相关 [13] 。因此,研究中枢炎症的发病机制
而部分抑制炎症介质的释放。 及防治策略对于治疗 CNS 疾病及改善患者的预后
2.4 α⁃FMH可缓解LPS诱导的大鼠恐惧记忆损伤 具有深远的意义。本课题组先前已经报道过原代
如前所述α⁃FMH可以降低MG的激活并能抑制 培养的MG表达4种类型的组胺受体,其中组胺可上
炎症介质的释放从而减轻中枢炎症,而认知功能障 调 H1R 和 H4R 的表达,诱导 MG 活化,进而释放炎
碍是术后中枢炎症的常见并发症。为此我们进行 症因子如IL⁃6和TNF⁃α [11] 。然而动物实验关于组胺
在 LPS 诱导的 MG 激活、神经炎症和认知障碍中的
A 作用尚未得到阐明。本研究发现,α⁃FMH可以抑制
600
* LPS诱导的MG活化和神经炎症,并减轻了大鼠的认
( pg/mL) 400 *# 知功能障碍。
神经科学研究发现免疫系统和 CNS 之间存在
TNF⁃α 200 双向信息交流,MG 释放的促炎因子在这种交流中
0 起着关键作用。MG的激活是神经元坏死及CNS退
Control α⁃FMH LPS α⁃FMH+LPS
行性疾病的早期预兆。研究发现LPS、组胺和IL⁃10
B 1 000
* 等多种物质均可以引起MG的激活,并诱导向M1表
800
( pg/mL) 600 型及 M2 表型之间转换 [14] 。组胺作为中枢重要的
神经递质其在 MG 介导的中枢炎症中发挥重要作
IL⁃6 400 *# 用 [15-16] 。脑组胺不仅存在于神经元中,也存在于大
200
脑肥大细胞中,Dong等 [17] 证实给予肥大细胞的稳定
0
Control α⁃FMH LPS α⁃FMH+LPS
剂可抑制 LPS 诱导的 MG 活化和神经炎症,并减轻
A:大鼠海马区 TNF⁃α的表达;B:大鼠海马区 IL⁃6 的表达。与
LPS诱导的认知功能障碍。此外早有在大鼠黑质中
Control组相比,P < 0.01;与LPS组相比,P < 0.01(n=4)。 [18]
*
#
图3 α⁃FMH对大鼠海马区炎症因子表达的影响 注射组胺可以诱导MG 活化的报道 。然而目前关
Figure 3 Effects of α⁃FMH on the expression of inflam⁃ 于 4 种组胺受体在 MG 介导的炎症中如何发挥作用
matory cytokines in rat hippocampus 尚未完全阐明。