Page 90 - 南京医科大学学报自然科学版
P. 90
第43卷第9期
·1268 · 南 京 医 科 大 学 学 报 2023年9月
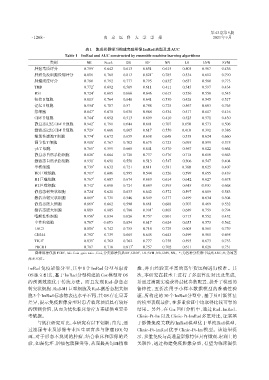
表1 集成机器学习构建免疫影像ImRad表型及其AUC
Table 1 ImRad and AUC constructed by ensemble machine learning algorithms
类别 NB Stack GB RF NN LR kNN SVM
肿瘤基质评分 0.759 * 0.642 0.613 0.651 0.615 0.503 0.567 0.436
肿瘤免疫细胞浸润评分 0.806 * 0.760 0.813 0.821 * 0.785 0.534 0.612 0.790
肿瘤纯度评分 0.780 * 0.792 0.777 0.795 0.832 * 0.637 0.580 0.773
TMB 0.772 * 0.692 0.569 0.611 0.411 0.545 0.597 0.434
*
MSI 0.724 0.685 0.666 0.646 0.615 0.556 0.558 0.545
初始B细胞 0.813 * 0.764 0.648 0.641 0.530 0.428 0.545 0.517
记忆B细胞 0.954 * 0.787 0.57 0.788 0.725 0.567 0.683 0.765
浆细胞 0.847 * 0.670 0.638 0.584 0.534 0.517 0.607 0.416
CD8 T细胞 0.744 * 0.692 0.513 0.609 0.410 0.523 0.571 0.430
+
静息态记忆CD4 T细胞 0.942 * 0.791 0.644 0.801 0.707 0.650 0.573 0.506
+
激活态记忆CD4 T细胞 0.729 * 0.666 0.605 0.617 0.550 0.410 0.392 0.386
+
辅助性滤泡T细胞 0.774 * 0.672 0.659 0.698 0.648 0.538 0.624 0.660
调节性T细胞 0.908 * 0.767 0.702 0.675 0.723 0.695 0.599 0.575
γδ T 细胞 0.765 * 0.599 0.668 0.641 0.570 0.567 0.622 0.664
静息态自然杀伤细胞 0.820 * 0.664 0.728 0.737 0.576 0.718 0.616 0.663
激活态自然杀伤细胞 0.931 * 0.691 0.558 0.513 0.547 0.306 0.547 0.404
单核细胞 0.739 * 0.632 0.721 0.611 0.581 0.380 0.625 0.407
M0巨噬细胞 0.717 * 0.606 0.595 0.544 0.526 0.599 0.655 0.439
M1巨噬细胞 0.767 * 0.607 0.674 0.669 0.614 0.642 0.627 0.678
M2巨噬细胞 0.742 * 0.698 0.724 0.689 0.595 0.645 0.590 0.668
静息态树突状细胞 0.724 * 0.621 0.633 0.642 0.572 0.597 0.609 0.583
激活态树突状细胞 0.869 * 0.731 0.546 0.549 0.377 0.499 0.634 0.504
静息态肥大细胞 0.869 * 0.662 0.590 0.661 0.688 0.707 0.469 0.532
激活态肥大细胞 0.889 * 0.805 0.786 0.901 * 0.803 0.689 0.759 0.794
嗜酸性粒细胞 0.956 # 0.834 0.626 0.757 0.801 0.715 0.552 0.432
中性粒细胞 0.767 * 0.670 0.654 0.617 0.624 0.655 0.573 0.562
LAG3 0.806 * 0.742 0.755 0.714 0.729 0.605 0.561 0.739
*
CD244 0.752 0.739 0.665 0.645 0.643 0.499 0.561 0.695
TIGIT 0.835 * 0.762 0.762 0.777 0.758 0.593 0.673 0.753
PDCD1 0.787 * 0.718 0.817 * 0.757 0.702 0.611 0.628 0.731
降维算法包括FCBF、Info.Gain、gain ratio、Gini,分类算法包括RF、GBDT、LR、SVM、NB、kNN、NN。*:为各种分类器中最高AUC;#:为显著
高AUC值。
ImRad 免疫影像分型,其中 8 个 ImRad 分型与患者 性,并由经验更丰富的高年资医师进行校准。其
OS独立相关,基于ImRad分型构建的Cox模型对OS 次,本研究在技术上进行了多重算法对比及集成,
的预测效能优于传统方法。而且发现 Rad⁃静息态 并通过消融实验获得最优参数配置,提升了模型的
树突状细胞、Rad⁃M1巨噬细胞及Rad⁃激活态肥大细 鲁棒性,五折法用于小样本数据模型的准确性验
胞3个ImRad标志物表达水平不同,其OS存在显著 证,所构建的 30 个 ImRad 分型中,基于贝叶斯算法
差异,提示免疫影像分型对患者临床预后具有较好 的模型表现最佳,在多重验证中均取得比较可靠的
的预测价值,从而为优化临床治疗方案提供重要参 结果。另外,在 Cox 回归分析中,通过 Rad、ImRad、
考依据。 Clinic⁃Pt⁃Im 以及 Clinic⁃Pt⁃ImRad 多重对比,证实基
与既往研究对比,本研究有以下创新:首先,通 于影像免疫关联的 ImRad 模型优于单纯 Rad 模型,
过泌尿专业及影像专业医生双盲参与肿瘤 ROI 勾 Clinic⁃Pt⁃ImRad 优于 Clinic⁃Pt⁃Im 模型。该结果提
画,对于形态不规则的肿瘤,结合临床和影像的经 示,多重免疫与高通量影像特征具有微观⁃宏观上的
验,如强化环、肿瘤包膜隆突等,从而提高勾画精准 关联性,通过构建免疫影像分型,有望为临床提供