Page 50 - 南京医科大学学报自然科学版
P. 50
第41卷第7期
·980 · 南 京 医 科 大 学 学 报 2021年7月
A B
空白对照组 干扰对照组 干扰GDF15组 G2/M期
150
S期 *
( % ) G1期 *
未放射 细胞周期 100
50
0
2 N 4 N 2 N 4 N 2 N 4 N 未放射 放射后3 d
A C
2.0 空白对照组
干扰对照组
h 1.5 干扰GDF15组
放射后24 nm ) 1.0 **
( 450
D
0.5 **
2 N 4 N 2 N 4 N 2 N 4 N 0
未放射 放射后3 d
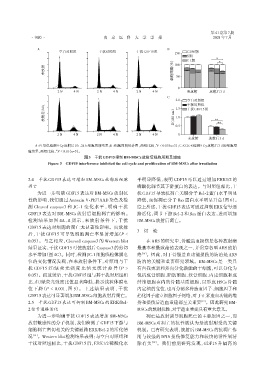
A:PI染色检测9 Gy放射后0 h、24 h细胞周期结果;B:细胞周期统计图,两组比较,P ˂ 0.05(n=3);C:CCK⁃8检测9 Gy放射后3 d的细胞增
*
殖结果,两组比较,P ˂ 0.01(n=5)。
**
图3 干扰GDF15抑制BM⁃MSCs放射后细胞周期及增殖
Figure 3 GDF15 interference inhibited the cell cycle and proliferation of BM⁃MSCs after irradiation
2.4 干扰GDF15表达可增加BM⁃MSCs放射后细胞 平明显降低,表明 GDF15 可以通过增加 ERK1/2 的
凋亡 磷酸化调节其下游蛋白的表达。与对照组相比,干
为进一步明确 GDF15 表达对 BM⁃MSCs 放射抗 扰GDF15导致抗凋亡关键分子Bcl⁃2蛋白水平明显
性的影响,我们通过 Annexin V⁃PE/7AAD 染色及检 降低,而促凋亡分子 Bax 蛋白水平明显升高(图 6)。
测 Cleaved caspase3 和 JC⁃1 变化水平,明确干扰 综上所述,干扰GDF15表达可通过抑制ERK信号通
GDF15 表达对 BM⁃MSCs 放射后细胞凋亡的影响。 路活化,调节下游 Bcl⁃2 和 Bax 蛋白表达,进而增加
检测结果如图 4A、B 所示,未放射条件下,干扰 BM⁃MSCs放射后凋亡。
GDF15 表达对细胞的凋亡无显著性影响。而放射
3 讨 论
后,干扰 GDF15 可导致细胞凋亡率显著增加(P ˂
0.05)。与之相应,Cleaved caspase3 的 Western blot 在ARS的研究中,骨髓造血损伤是各种放射病
结果证实,干扰GDF15可使放射后Caspase3的剪切 最基本和最致命的表现之一,并贯穿各型ARS的始
水平增加(图4C)。同时,检测JC⁃1细胞线粒体膜电 终 [16] 。因此,对于骨髓造血功能损伤的防治是ARS
位的变化情况发现,在未放射条件下,对照组与干 防治的关键和重要研究领域。BM⁃MSCs 是一类具
扰 GDF15 红/绿 荧 光 强 度 比 值 无 统 计 差 异(P ˃ 有自我更新和多向分化潜能的干细胞,可以分化为
0.05)。而放射后,干扰GDF15组与其干扰对照组相 包括成骨细胞、脂肪细胞、软骨细胞、内皮细胞和成
比,红/绿荧光强度比值显著降低,提示线粒体膜电 纤维细胞在内的骨髓基质细胞,以形成 HSCs 骨髓
位下降(P ˂ 0.001,图 5)。上述结果表明,干扰 内定植的龛位,也可分泌多种造血因子、细胞因子和
GDF15表达可显著增加BM⁃MSCs细胞放射后凋亡。 趋化因子建立细胞因子网络,对于正常造血功能的维
[17]
2.5 干扰GDF15表达可抑制BM⁃MSCs 的ERK/Bcl⁃ 持和损伤后造血重建都至关重要 。因此研究BM⁃
2信号通路活化 MSCs的放射抗性,对于造血重建具有重大意义。
为进一步明确干扰 GDF15 表达增加 BM⁃MSCs 凋亡是放射诱导细胞死亡的主要原因之一,而
放射敏感性的分子机制,我们检测了GDF15下游与 BM⁃MSCs 对凋亡的抗性被认为是放射耐受的关键
细胞凋亡密切相关的关键通路ERK/Bcl⁃2的活化情 机制。已有研究表明,放射后BM⁃MSCs的抗凋亡作
况 [15] 。Western blot检测结果表明:与空白对照组和 用与较强的 DNA 损伤修复能力和较快的活性氧清
干扰对照组相比,干扰 GDF15 后,ERK1/2 磷酸化水 除有关 [18] 。我们前期研究发现,GDF15 升幅高的