Page 17 - 《南京医科大学学报》2026年第1期
P. 17
第46卷第1期 徐 甲,厉梦琪,袁小琴. 肿瘤相关成纤维细胞分泌THBS2通过PI3K/AKT通路驱动巨噬
2026年1月 细胞M2极化促进结直肠癌进展[J]. 南京医科大学学报(自然科学版),2026,46(1):1-13 · 11 ·
A M0 IL⁃4
Relative ARG1 expression Relative p⁃PII3K/PI3K expression 1.0 Relative p⁃AKT/AKT expression 1.0
ARG1 35 kDa 2.5 * 2.0 * 2.5 *
p⁃PI3K 85 kDa 2.0 1.5 2.0
PI3K 85 kDa 1.5 1.5
p⁃AKT 60 kDa 1.0 0.5 0.5
AKT 60 kDa 0.5 0 0 0
β⁃actin 43 kDa M0 IL⁃4 M0 IL⁃4 M0 IL⁃4
NF⁃CM CAF⁃CM
B
ARG1 35 kDa 6 * 2.0 * 2.0 *
p⁃PI3K 85 kDa 2 1.5 1.5
PI3K 85 kDa Relative ARG1 expression Relative p⁃PII3K/PI3K expression 1.0 Relative p⁃AKT/AKT expression 1.0
p⁃AKT 60 kDa 1 0.5 0.5
AKT 60 kDa 0 0 0
β⁃actin 43 kDa NF⁃CM CAF⁃CM NF⁃CM CAF⁃CM NF⁃CM CAF⁃CM
M0 *
C IL⁃4 THBS2
Relative ARG1 expression Relative p⁃PII3K/PI3K expression Relative p⁃AKT/AKT expression
ARG1 35 kDa 6 * 2.5 * 3 *
p⁃PI3K 85 kDa * 2.0 * * *
PI3K 85 kDa 2 * 1.5 2
p⁃AKT 60 kDa 1 1.0 1
0.5
AKT 60 kDa 0 0 0
β⁃actin 43 kDa M0 IL⁃4 THBS2 M0 IL⁃4 THBS2 M0 IL⁃4 THBS2
si⁃nc⁃CM si⁃2⁃CM si⁃3⁃CM
D
Relative ARG1 expression
ARG1 35 kDa 1.5 * 1.5 * 1.5 *
p⁃PI3K 85 kDa 1.0 * 1.0 * 1.0 *
PI3K 85 kDa 0.5 Relative p⁃PII3K/PI3K expression 0.5 Relative p⁃AKT/AKT expression 0.5
p⁃AKT 60 kDa
AKT 60 kDa 0 0 0
β⁃actin 43 kDa si⁃nc⁃CM si⁃2⁃CM si⁃3⁃CM si⁃nc⁃CM si⁃2⁃CM si⁃3⁃CM si⁃nc⁃CM si⁃2⁃CM si⁃3⁃CM
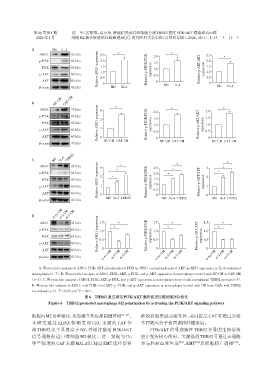
A:Western blot analysis of ARG1,PI3K,AKT,phosphorylated PI3K(p⁃PI3K),and phosphorylated AKT(p⁃AKT)expression in IL⁃4⁃stimulated
macrophages(n=3). B:Western blot analysis of ARG1,PI3K,AKT,p⁃PI3K,and p⁃AKT expression in macrophages treated with NF⁃CM or CAF⁃CM
(n=3). C:Western blot analysis of ARG1,PI3K,AKT,p⁃PI3K,and p⁃AKT expression in macrophages treated with recombinant THBS2 protein(n=3).
D:Western blot analysis of ARG1,total PI3K,total AKT,p⁃PI3K,and p⁃AKT expression in macrophages treated with CM from CAFs with THBS2
*
**
knockdown(n=3). P < 0.05 and P < 0.01.
图6 THBS2通过激活PI3K/AKT通路促进巨噬细胞M2极化
Figure 6 THBS2 promoted macrophage M2 polarization by activating the PI3K/AKT signaling pathway
细胞向M2表型极化,从而建立免疫抑制微环境 [23-24] 。 移的机制形成功能互补,共同提示CAF可通过分泌
本研究通过 ELISA 检测发现 CRC 来源的 CAF 分 不同效应分子协同调控肿瘤进展。
泌 THBS2 水平显著高于 NF,并通过激活 PI3K/AKT PI3K/AKT 信号通路在 THBS2 介导的生物学效
信号通路促进巨噬细胞 M2 极化。这一发现与 Hu 应中发挥核心作用。文献报道THBS2可通过该通路
等 [21] 报道的 CAF 来源 MALAT1 通过 EMT 途径促转 参与肿瘤血管生成 [25] 、EMT [26] 及细胞凋亡调控 [27] 。