Page 61 - 《南京医科大学学报》自然科学版2026年第2期
P. 61
第46卷第2期 沈链链,管强东,丁竞竞,等. 微孔板成像系统在高表达荧光蛋白单克隆细胞株筛选中的应用[J].
2026年2月 南京医科大学学报(自然科学版),2026,46(2):213-220 ·217 ·
Stably transfected cells Monoclonal cell strain 1 Monoclonal cell strain 2 Monoclonal cell strain 3
250 250 250 250
(×10 3 ) 200 15.7% (×10 3 ) 200 99.8% (×10 3 ) 200 97.7% (×10 3 ) 200 99.4%
GFP+
GFP+
GFP+
GFP+
150
150
150
150
SSC⁃A 100 SSC⁃A 100 SSC⁃A 100 SSC⁃A 100
50 50 50 50
0 0 0 0
0 10 3 10 4 10 5 0 10 3 10 4 10 5 0 10 3 10 4 10 5 0 10 3 10 4 10 5
GFP⁃A GFP⁃A GFP⁃A GFP⁃A
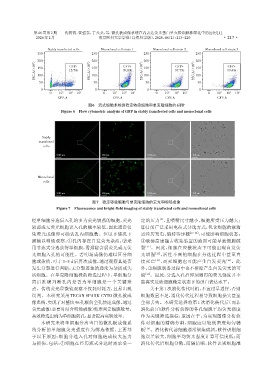
图6 流式细胞术检测稳定转染细胞和单克隆细胞的GFP
Figure 6 Flow cytometric analysis of GFP in stably transfected cells and monoclonal cells
Stably
transfected
cells
Monoclonal
cells
图7 稳定转染细胞与单克隆细胞的荧光和明场成像
Figure 7 Fluorescence and bright⁃field imaging of stably transfected cells and monoclonal cells
经单细胞分选后入孔的多为荧光较强的细胞,荧光 定的压力 ,且喷嘴尺寸越小,细胞所受压力越大;
[9]
较弱或无荧光细胞误入孔的概率较低,因此通常仅 ②目前广泛采用电荷式分选方式,包含细胞的液滴
凭荧光成像即可确认孔内细胞数。但以下情况下 需经历充电、偏转等步骤 [19-20] ,可能影响细胞状态;
需辅以明场观察:①孔内存在自发荧光杂质;②采 ③液滴高速撞击收集装置的液面可能导致细胞破
用非流式分选获得单细胞,需排除含弱荧光或无荧 裂 [21] 。因此,细胞在应激状态下可能出现自发荧
光细胞入孔的可能性。若明场成像仍难以区分细 光增强 [22] ,活性不高的细胞在分选过程中甚至直
胞或杂质,可于3~5 d后再次成像,通过观察其是否 接死亡 [23] ,而死细胞也可能产生自发荧光 [24] 。此
发生分裂进行判断,无分裂迹象的通常为杂质或失 外,单细胞制备过程中也不排除产生自发荧光的可
活细胞。在单克隆细胞株的筛选过程中,单细胞分 能 [25] 。因此,分选入孔后即刻测得的荧光强度并不
离后准确判断孔内是否为单细胞是一个关键难 能真实反映细胞稳定状态下的蛋白表达水平。
点。传统荧光显微镜观察不仅耗时耗力,且易出现 关于第1次消化传代时机,不宜过早进行,否则
误判。本研究采用 TECAN SPARK CYTO 微孔板成 细胞数量不足,消化传代过程易导致细胞损失甚至
像系统,实现了对整块96孔板的全孔快速成像,通过 全部丢失。本研究选择将第 1 次消化传代后(而非
荧光成像(必要时结合明场成像)精准判定细胞数量, 消化前)由软件分析获得的各孔细胞平均荧光强度
高效筛选出确为单细胞的孔,显著提高实验效率。 作为关键筛选指标,原因在于:为实现图像分析软
本研究未将单细胞分离当日的微孔板成像系 件对细胞的精确分割,细胞应以较低密度均匀铺
统分析的单细胞荧光强度作为筛选依据,主要基 板 [26] 。消化传代前细胞通常聚集成团,软件识别细
于以下原因:细胞分选入孔对细胞造成较大压力 胞误差较大,细胞平均荧光强度计算可信度低;而
与损伤,包括:①细胞在经历流式分选时需承受一 消化传代后细胞分散、间隔清晰,软件识别细胞准