Page 59 - 《南京医科大学学报》自然科学版2026年第2期
P. 59
第46卷第2期 沈链链,管强东,丁竞竞,等. 微孔板成像系统在高表达荧光蛋白单克隆细胞株筛选中的应用[J].
2026年2月 南京医科大学学报(自然科学版),2026,46(2):213-220 ·215 ·
孔用于后续成像参数优化,其余95个孔均设置分选 胞株。上述过程细胞培养基均不含嘌呤霉素。
1个细胞入孔用于单克隆筛选。 1.2.5 单克隆细胞株的扩大培养与荧光强度验证
1.2.3 微孔板成像系统操作 继续培养筛选出的细胞株,通过数次消化传代
使用 TECAN SPARK CYTO 进行成像与分析。 将其转移至新的孔或更大的孔或培养皿中培养。自
①成像:使用“Fluorescence Imaging”功能进行荧光 分选后持续培养稳定转染细胞,培养条件与单克隆
和明场成像,4 倍物镜,全孔成像。预先使用 D7 孔 细胞一致(均不含嘌呤霉素)。待单克隆细胞增殖至
预览图像并优化成像参数。②图像查看:通过分析 细胞数足够时,对稳定转染细胞及单克隆细胞株,使
软件打开自动生成的实验文件,可点击查看任意孔 用BD LSRFortessa流式细胞仪进行GFP荧光强度检
的全孔荧光和明场成像。③数据分析:成像结束后 测;将等量细胞接种于96孔板,利用微孔板成像系统
系统自动完成初步分析,数据导出至 Excel 表格。 再次进行明场与荧光成像,直观比较荧光信号强弱。
必要时可调整参数后重新分析。
2 结 果
1.2.4 单克隆细胞株筛选流程
①筛选单细胞孔:单细胞分离当天,利用微孔 2.1 筛选单细胞孔
板成像系统的成像功能,观察荧光成像和明场成 分选完成后1~2 h,待细胞沉底后即用微孔板成
像,筛选出有且仅有 1 个细胞的孔。②筛选生成克 像系统成像,虽然分析软件能自动分析每孔内细胞
隆团的孔:待大多数能生成克隆团的孔已有较大的 数,但由于孔内可能有杂质,或者细胞形态稍有异常
克隆团(>20 个细胞)时,再次进行成像,筛选出具 等原因,导致有些孔的细胞数量分析不准确,因此并
有明显克隆团的孔。③细胞消化传代:将筛选出的 不建议直接采用细胞数量分析结果,而以肉眼观察荧
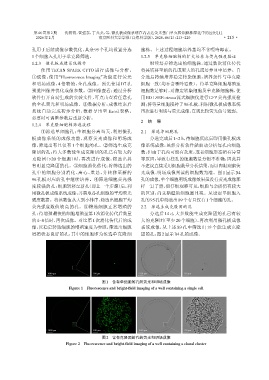
孔中的细胞分别消化、离心、重悬,并转移至新的 光成像、明场成像判读的细胞数为准。图1显示B4
96 孔板对应的孔中继续培养。④筛选细胞荧光强 孔的成像,单个细胞明场成像效果虽没有荧光成像那
度较强的孔:细胞转移至新孔(即上一个步骤)后,利 样一目了然,但仔细观察可见,细胞与杂质仍有较大
用微孔板成像系统成像,并获取各孔细胞的平均荧光 的区别,尚未贴壁的细胞圆且亮。从设定单细胞入
强度数据。将该数值从大到小排序,筛选出细胞平均 孔的95孔中筛选出89个有且仅有1个细胞的孔。
荧光强度数值较高的孔。⑤筛选细胞正常增殖的 2.2 筛选生成克隆团的孔
孔:待增殖最快的细胞增殖至第1次消化传代后数量 分选后 14 d,大多数能生成克隆团的孔已有较
的4~8倍时,再次成像。对比第1次消化传代后的成 大的克隆团(至少20个细胞),再次利用微孔板成像
像,以稳定转染细胞的增殖速度为参照,筛选出细胞 系统成像,从上述 89 孔中筛选出 19 个能生成克隆
增殖状态良好的孔,其中的细胞即为候选单克隆细 团的孔,图2显示B4孔的成像。
图1 含有单细胞的孔的荧光和明场成像
Figure 1 Fluorescence and bright⁃field imaging of a well containing a single cell
图2 含有克隆团的孔的荧光和明场成像
Figure 2 Fluorescence and bright⁃field imaging of a well containing a clonal cluster