Page 44 - 南京医科大学自然科学版第1期
P. 44
第41卷第1期
· 38 · 南 京 医 科 大 学 学 报 2021年1月
苦参碱浓度(g/L)
**
0 0.4 0.8
*
900
800
( 个 ) 700
600
迁移细胞数 500
400
300
200
100
0
0 0.4 0.8
苦参碱浓度(g/L)
两组相比,P<0.05,P<0.01,n=6。
**
*
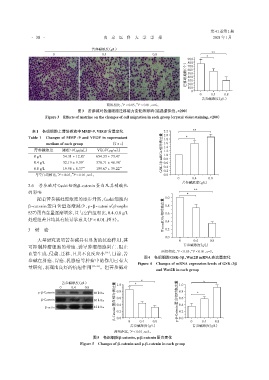
图3 苦参碱对各组细胞迁移能力变化的影响(结晶紫染色,×200)
Figure 3 Effects of matrine on the changes of cell migration in each group(crystal violet staining,×200)
表1 各组细胞上清培养液中MMP⁃9、VEGF含量变化 **
Table 1 Changes of MMP ⁃ 9 and VEGF in supernatant 2.0 *
1.8
medium of each group (x ± s) mRNA相对表达量 2.2
1.6
苦参碱浓度 MMP⁃9(ng/mL) VEGF(pg/mL) 1.4
1.2
0 g/L 54.31 ± 12.87 ** 654.33 ± 73.47 1.0
0.8
**
0.4 g/L 32.19 ± 9.39 0 378.71 ± 48.98 * 0.6
**
0.8 g/L 19.96 ± 6.37 0 159.67 ± 39.22 ** GSK⁃3β 0.4
0.2
与空白组相比,P<0.05,P<0.01,n=3。 0.0
**
*
0 0.4 0.8
苦参碱浓度(g/L)
2.6 苦参碱对Caski细胞β⁃catenin蛋白及其磷酸化
**
的影响
*
随着苦参碱处理浓度的逐步升高,Caski细胞内
β⁃catenin 蛋白含量逐渐减少,p⁃β⁃catenin(phospho 0.8
S37)蛋白含量逐渐增多,且与空白组相比,0.4、0.8 g/L Wnt mRNA相对表达量 1.0
0.6
处理组差异均具有统计学意义(P<0.01,图5)。 0.4
3 讨 论 0.2
0.0
大量研究表明苦参碱具有显著的抗癌作用,其 0 0.4 0.8
苦参碱浓度(g/L)
可抑制肿瘤细胞的增殖、诱导肿瘤细胞凋亡、阻止
两组相比,P<0.05,P<0.01,n=3。
*
**
血管生成、侵袭、迁移,且其不良反应小 [16] ,目前,苦
图4 各组细胞GSK⁃3β、Wnt2B mRNA表达量变化
参碱在肝癌、胃癌、乳腺癌等肿瘤中的作用已有大
Figure 4 Changes of mRNA expression levels of GSK⁃3β
量研究,表现出良好的抗癌作用 [17-19] 。但苦参碱对 and Wnt2B in each group
*
苦参碱浓度(g/L) 1.0 * 1.0 *
β⁃Catenin蛋白相对表达量 p⁃β⁃Catenin蛋白相对表达量
0 0.4 0.8
p⁃β⁃Catenin 86 kDa 0.8 0.8 *
β⁃Catenin 86 kDa 0.6 0.6
β⁃actin 42 kDa 0.4 0.4
0.2
0.2
0.0
0 0.4 0.8 0.0 0 0.4 0.8
苦参碱浓度(g/L) 苦参碱浓度(g/L)
两组相比,P<0.01,n=3。
*
图5 各组细胞β⁃catenin、p⁃β⁃catenin蛋白变化
Figure 5 Changes of β⁃catenin and p⁃β⁃catenin in each group