Page 41 - 南京医科大学学报自然科学版
P. 41
第41卷第3期 周阳春,章 静,朱 峰. 水通道蛋白3参与缺氧介导的结直肠癌化疗耐药的机制研究[J].
2021年3月 南京医科大学学报(自然科学版),2021,41(03):344-348 ·347 ·
A B
120 150
常氧 *
( % ) 100 * * * 缺氧 ( % ) 100 * *
80
细胞活力 60 细胞活力 50
40
20
0 0
缺氧+5⁃Fu
缺氧+si⁃Ctrl+5⁃Fu
0 20 40 80 常氧
5⁃Fu(μg/mL) 常氧+5⁃Fu 缺氧+si⁃AQP3+5⁃Fu
C D
常氧+5⁃Fu 缺氧+5⁃Fu 缺氧+si⁃Ctrl+5⁃Fu 缺氧+si⁃AQP3+5⁃Fu
200
* *
克隆数 100
0
缺氧+si⁃Ctrl+5⁃Fu
常氧+5⁃Fu 缺氧+5⁃Fu
缺氧+si⁃AQP3+5⁃Fu
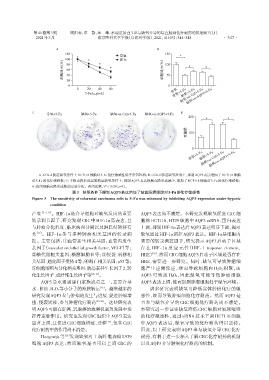
A:CCK⁃8验证缺氧条件下HCT116细胞对5⁃Fu化疗敏感性低于常氧环境;B:CCK⁃8验证缺氧环境下,抑制AQP3表达增加了HCT116细胞
对5⁃Fu的化疗敏感性;C:平板克隆形成实验验证缺氧条件下,抑制AQP3表达细胞克隆形成减少,增加了HCT116细胞对5⁃Fu的化疗敏感性;
D:各组细胞克隆形成数的定量分析。两组比较,P < 0.05(n=3)。
*
图3 缺氧条件下抑制AQP3表达增加了结直肠癌细胞对5⁃Fu的化疗敏感性
Figure 3 The sensitivity of colorectal carcinoma cells to 5⁃Fu was enhenced by inhibiting AQP3 expression under hypoxic
condition
产生 [5-6,8] 。HIF⁃1α是介导细胞对缺氧反应的重要 AQP3表达尚不清楚。本研究发现缺氧促进CRC细
转录调节因子,研究发现 CRC 中 HIF⁃1α高表达,且 胞株 HCT116、HT29 细胞中 AQP3 mRNA、蛋白表达
与肿瘤分化程度、临床病理分期以及淋巴结转移有 上调,抑制HIF⁃1α表达后AQP3表达明显下调,提示
关 [19] 。HIF⁃1α参与多种肿瘤相关基因的转录调 缺氧通过HIF⁃1α调控AQP3表达。HIF⁃1α是细胞内
控。主要包括:①血管新生相关基因:血管内皮生 重要的转录调控因子,研究提示 AQP3 启动子区域
长因子(vascular endothelial growth factor,VEGF)等; 存 在 HIF ⁃ 1α 反 应 元 件(HIF ⁃ 1 response element,
[18]
②糖代谢相关基因:糖酵解酶Ⅱ等;③侵袭、转移相 HRE) ,然而CRC细胞AQP3启动子区域是否存在
关基因:趋化因子受体4等;④凋亡相关基因:p53等; HRE,需要进一步研究。同时,缺氧可导致肿瘤细
⑤细胞增殖与分化相关基因:胰岛素样生长因子2、转 胞产生应激反应,继而导致细胞内 H2O2 积聚,而
化生长因子、成纤维生长因子等 [20-21] 。 AQP3 可转运 H2O2,因此缺氧可能导致肿瘤细胞
AQP3 是水通道蛋白家族成员之一,主要介导 AQP3表达上调,继而加剧肿瘤细胞处于缺氧环境。
水、甘油、H2O2等小分子的跨膜转运 。越来越多的 诸多研究表明缺氧可降低实体肿瘤化疗的敏
[22]
研究发现AQP3参与肿瘤的发生与进展,促进肿瘤增 感性,继而导致肿瘤细胞化疗耐药。然而 AQP3 是
殖、侵袭转移,参与肿瘤化疗耐药 [23-24] 。这些研究表 否参与缺氧介导的 CRC 细胞化疗耐药尚不清楚。
明AQP3可能在肝癌、乳腺癌的致癌机制及发展中发 本研究进一步证实缺氧降低 CRC 细胞对氟尿嘧啶
挥着重要作用。研究也发现CRC 组织中AQP3表达 的化疗敏感性,通过 siRNA 技术下调 HCT116 细胞
[17]
显著上调,且促进CRC 细胞增殖、迁移 ,但在CRC 中 AQP3 表达后,缺氧导致的化疗耐药得以逆转。
化疗耐药中的作用尚不清楚。 因此,以上研究表明 AQP3 参与缺氧介导 CRC 化疗
Hoogewijs 等 [18] 发现缺氧可上调纤维肉瘤 L929 耐药,有利于进一步深入了解CRC化疗耐药的机制
细胞 AQP3 表达;然而缺氧是否可以上调 CRC 的 以及AQP3介导肿瘤化疗耐药的机制。