Page 31 - 南京医科大学学报自然科学版
P. 31
第43卷第2期 朱伯谦,宋兵战,陈 凯,等. DNA甲基化调控p16表达在替格瑞洛改善血管内皮功能中的
2023年2月 作用及机制[J]. 南京医科大学学报(自然科学版),2023,43(2):169-178 ·173 ·
2.3 替格瑞洛对ox⁃LDL诱导的HUVEC p16表达的 A
3.0 *
影响 * *
为研究替格瑞洛对 ox⁃LDL 诱导的 HUVEC p16 2.0
表达的影响,通过real⁃time PCR 和Western blot实验 mRNA相对表达量
分别检测 p16 表达情况,发现 ox⁃LDL 可使 HUVEC 1.0
中 p16 mRNA 及蛋白表达上调(P < 0.01,图 2A、B),
p16
而替格瑞洛干预后,ox⁃LDL 诱导的 HUVEC p16
0
mRNA 及蛋白表达显著降低(P < 0.01,图 2A、B)。 ox⁃LDL - + + + +
Ti.(μmol/L) - - 10 20 40
以上结果显示,替格瑞洛可抑制ox⁃LDL诱导的HU⁃
B
VEC中p16的表达。 ox⁃LDL - + +
Ti.(μmol/L) - - 40
2.4 p16过表达与敲除系统的构建
p16 18 kDa
为研究 p16 过表达与敲除系统的有效性,通过
real⁃time PCR和Western blot实验分别检测p16表达 β⁃actin 42 kDa
情况,发现与对照组相比,p16过表达显著升高HU⁃
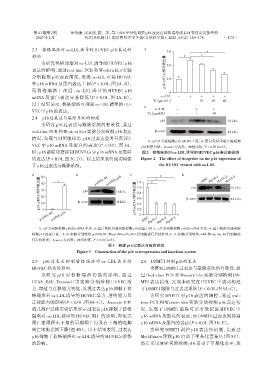
A:qPCR 实验检测 p16 mRNA 丰度;B:蛋白免疫印迹实验检测
VEC 中 p16 mRNA 及蛋白的表达(P < 0.01,图 3A、 p16的蛋白量。β⁃actin为内参。两组比较,P < 0.01(n=3)。
*
B);p16敲除显著抑制HUVECs中p16 mRNA及蛋白 图2 替格瑞洛对ox⁃LDL诱导的HUVEC p16表达的影响
的表达(P < 0.01,图3C、D)。以上结果表明成功构建 Figure 2 The effect of ticagrelor on the p16 expression of
了p16过表达与敲除系统。 the HUVEC treated with ox⁃LDL
A 50 * B pcDNA⁃NC pcDNA⁃p16 C 1.2 * * * D shNC shp16⁃1 shp16⁃2 shp16⁃3
mRNA相对表达量 40 p16 18 kDa mRNA相对表达量 1.0 β⁃actin 18 kDa
p16
30
0.8
20
0.6
42 kDa
p16 10 0 β⁃actin 42 kDa 0.4
0.2
pcDNA⁃NC pcDNA⁃p16 p16 0 shNC shp16⁃1 shp16⁃2 shp16⁃3
A:qPCR实验检测p16的mRNA丰度;B:蛋白免疫印迹实验检测p16的蛋白量;C:qPCR实验检测p16的mRNA丰度;D:蛋白免疫印迹实验
检测p16的蛋白量。A、B:细胞分别转染pcDNA⁃NC和pcDNA⁃p16,48 h后细胞进行后续处理;C、D:细胞分别转染shNC和shp16s,48后细胞进
行后续处理。β⁃actin为内参。两组比较,P < 0.01(n=3)。
*
图3 构建p16过表达与敲除系统
Figure 3 Construction of the p16 overexpression and knockout system
2.5 p16 过表达抑制替格瑞洛对 ox⁃LDL 诱导的 2.6 DNMT1抑制p16的表达
HUVEC损伤的影响 为研究DNMT1过表达与敲除系统的有效性,通
为 研 究 p16 对 替 格 瑞 洛 功 能 的 影 响 ,通 过 过 Real⁃time PCR 和 Western blot 实验分别检测 DN⁃
CCK8、EdU、Transwell 等实验分别检测 HUVEC 活 MT1 表达情况,发现本研究在 HUVEC 中成功构建
力、增殖与迁移能力变化,发现过表达p16抑制了替 了DNMT1敲除与过表达系统(P < 0.01,图5A~C)。
格瑞洛对 ox⁃LDL 诱导的 HUVEC 活力、增殖能力及 为研究 DNMT1 对 p16 表达的调控,通过 real⁃
迁移能力的影响(P < 0.01,图4A~C)。Annexin V/PI time PCR 和 Western blot 实验分别检测 p16 表达情
流式凋亡迁移实验结果显示过表达p16抑制了替格 况,发现了 DNMT1 敲除可以有效促进 HUVEC 中
瑞洛对 ox⁃LDL 诱导的 HUVEC 凋亡的影响,即流式 p16 mRNA 及蛋白的表达;而 DNMT1 过表达则抑制
凋亡象限图右下角的早期凋亡以及右上角的晚期 p16 mRNA及蛋白的表达(P < 0.01,图5D、E)。
凋亡细胞比例下降(图4D)。以上结果表明,过表达 为研究 DNMT1 调控 p16 表达的机制,先通过
p16抑制了替格瑞洛对ox⁃LDL诱导的HUVECs损伤 MethPrimer 预测 p16 启动子甲基化富集区(图 5F),
的影响。 然后采用 MSP 实验检测 p16 启动子甲基化水平,发