Page 78 - 南京医科大学学报自然科学版
P. 78
第43卷第5期
·660 · 南 京 医 科 大 学 学 报 2023年5月
A 2.0
RhoA相对表达水平 1.0
对照 Tr AP Tr+FS AP+FS FS * *
RhoA 22 kDa 1.5 △ #
GAPDH 36 kDa 0.5
0
对照 Tr AP Tr+FS AP+FS FS
B 对照 Tr AP Tr+Y AP+Y Y
Hoechst 150
( % ) 100 △ #
细胞增殖率 50 * *
EdU
0
对照 Tr AP Tr+Y AP+Y Y
Merge
150
C ( % )
对照 Tr AP Tr+Y AP+Y Y 100 * * △ #
细胞迁移率 50
0
对照 Tr AP Tr+Y AP+Y Y
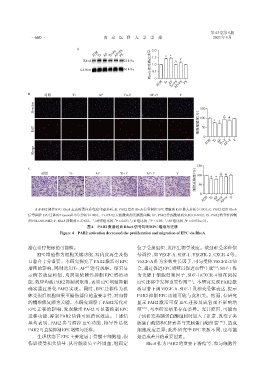
A:PAR2调控EPC RhoA表达的蛋白质免疫印迹分析;B:PAR2经由RhoA信号调控EPC增殖的EdU掺入分析(×100);C:PAR2经由RhoA
信号调控EPC迁移的Transwell小室分析(×100)。Tr:PAR2天然激动剂类胰蛋白酶;AP:PAR2合成激动剂SLIGKV⁃NH2;FS:PAR2特异性抑制
剂FSLLRY⁃NH2;Y:RhoA抑制剂Y⁃27632。与对照组比较,P < 0.05;与Tr组比较,P < 0.05;与AP组比较,P < 0.05(n=3)。
*
△
#
图4 PAR2激活经由RhoA信号抑制EPC增殖与迁移
Figure 4 PAR2 activation decreased the proliferation and migration of EPC via RhoA
潜在治疗靶标的可能性。 位于受损组织、发挥生物学效应。该过程受多种信
EPC 增殖作为细胞关键功能,对内皮再生及伤 号调控,如 VEGF⁃A、SDF⁃1、VEGFR⁃2、CXCR⁃4 等。
口愈合十分重要。本研究探究了PAR2激活对EPC VEGF⁃A 作为多效生长因子,可与受体 VEGFR⁃2 结
[15] [16]
增殖的影响,同时选用 Tr、AP 进行观察。结果显 合,通过促进EPC增殖以促进血管生成 ;SDF⁃1作
示两者效应相似,均剂量依赖性抑制 EPC 增殖功 为关键干细胞归巢因子,SDF⁃1/CXCR⁃4 轴在调控
能,效应均被PAR2抑制剂取消,表明EPC增殖抑制 EPC迁移中发挥重要作用 [17] 。本研究发现PAR2激
确实通过活化 PAR2 实现。同时,EPC 迁移作为机 活显著下调 VEGF⁃A、SDF⁃1 及相关受体表达,提示
体受损后细胞归巢至损伤部位的重要事件,对血管 PAR2抑制 EPC 功能可能与此相关。然而,有研究
的精准修复颇为关键。本研究观察了PAR2活化对 显示 PAR2 激活可促 EPC 迁移及成管而不影响增
EPC 迁移的影响,发现激活 PAR2 可显著抑制 EPC 殖 [18] ,与本研究结果存在差异。究其原因,可能由
迁移功能,抑制 PAR2 活性可取消该效应。上述结 于该研究类胰蛋白酶组同时加入了肝素,改变了类
[19]
果均表明,PAR2 参与调控 EPC 功能,特异性活化 胰蛋白酶结构(肝素参与类胰蛋白酶组装 ),造成
PAR2可直接抑制EPC增殖与迁移。 细胞反应差异;此外研究中 EPC 来源不同,也可能
生理状态下EPC 主要定居于骨髓干细胞池,损 是造成差异的重要因素。
伤后接受相关信号、从骨髓动员至外周血,继而定 RhoA 作为 PAR2 的重要下游信号,参与细胞骨