Page 38 - 南京医科大学学报自然科学版
P. 38
第43卷第7期
·924 · 南 京 医 科 大 学 学 报 2023年7月
A B C
4 3 ** ** 1.5 800 ***
B4GALT5相对表达量 2 * B4GALT5相对表达量 1.0 *** ** ** *** B4GALT5相对表达量 400 **
600
0.5
0 1 0 200 0 Vector OE Vector OE
sh⁃2
sh⁃1
sh⁃1
HPNE BxPC⁃3 CFPAC⁃1 MIA PaCa⁃2 PANC⁃1 sh⁃NC CFPAC⁃1 sh⁃3 sh⁃NC MIA PaCa⁃2 sh⁃3 CFPAC⁃1 MIA PaCa⁃2
sh⁃2
Vector OE
sh⁃NC sh⁃1 sh⁃2 sh⁃3 B4GALT5 45 kDa
PANC⁃1
HPNE BxPC⁃3 CFPAC⁃1 MIA PaCa⁃2 CFPAC⁃1 B4GALT5 45 kDa CFPAC⁃1 GAPDH 36 kDa
36 kDa
GAPDH
MIAPaCa⁃2 MIAPaCa⁃2
B4GALT5 45 kDa B4GALT5 45 kDa B4GALT5 45 kDa
36 kDa
GAPDH GAPDH 36 kDa GAPDH 36 kDa
B4GALT5蛋白相对表达量 4 3 2 1 * ** ** B4GALT5蛋白相对表达量 1.5 *** ** *** *** B4GALT5蛋白相对表达量 1 000 *** ***
800
1.0
600
400
0.5
200
0
sh⁃2
sh⁃1
HPNE BxPC⁃3 CFPAC⁃1 PANC⁃1 0 sh⁃NC CFPAC⁃1 sh⁃3 sh⁃NC sh⁃1 sh⁃2 sh⁃3 0 Vector OE Vector OE
MIA PaCa⁃2
CFPAC⁃1 MIA PaCa⁃2
MIA PaCa⁃2
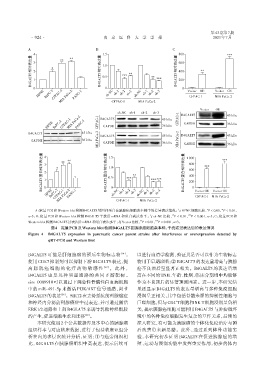
A:定量PCR和Western blot 检测B4GALT5基因和蛋白在胰腺癌细胞亲本株中的差异表达情况;与HPNE 细胞比较,P < 0.05,P < 0.01,
*
**
n=3;B:定量 PCR 和 Western blot 检测 B4GALT5 干扰后 mRNA 和蛋白表达水平;与 sh⁃NC 比较,P < 0.01, P < 0.001,n=3;C:定量 PCR 和
**
***
Western blot检测B4GALT5过表达后mRNA和蛋白表达水平;与Vector比较,P < 0.01, P < 0.001,n=3。
**
***
图4 定量PCR及Western blot检测B4GALT5在胰腺癌细胞亲本株、干扰或过表达后的表达情况
Figure 4 B4GALT5 expression in pancreatic cancer parent strains after interference or overexpression detected by
qRT⁃PCR and Western blot
B4GALT5 可能是肝细胞癌的预后生物标志物 [14] 。 以进行血清学检测,验证其是否可以作为生物标志
使用 CDK7 抑制剂可以抑制下游 B4GALT5 表达,提 物用于早期诊断;② B4GALT5的表达量增高与胰腺
高 膀 胱 癌 细 胞 的 化 疗 药 物 敏 感 性 [27] 。 此 外 , 癌不良预后呈显著正相关。B4GALT5 的表达量增
B4GALT5 也是几种明星通路的共同下游靶标。 高在不同的TNM、年龄、性别、临床分期组中均能够
circ_0009910可以通过下调急性骨髓性白血病细胞 作为不良预后的显著预测因素。进一步,本研究结
中的 miR⁃491⁃5p 来激活 PI3K/AKT 信号通路,调节 果还显示 B4GALT5 的表达量增高与多种免疫细胞
B4GALT5的表达 [28] 。SIRT2在去势抵抗前列腺癌症 浸润呈正相关,其中包括骨髓来源的抑制性细胞与
和神经内分泌前列腺癌症中过表达,并可通过激活 巨噬细胞,但与CD4 T细胞和NK T细胞浸润呈负相
+
ERK1/2通路和上调B4GLAT5来诱导乳糖神经酰胺 关,提示胰腺癌细胞可能利用B4GALT5与肿瘤微环
[29]
的产生,促进细胞生长和迁移 。 境中的各种免疫细胞发生复杂的互作关系,后续的
本研究使用2个公共数据库及本中心的胰腺癌 深入研究,有可能为胰腺癌的个体化免疫治疗与预
组织样本与对应临床数据,进行了包括临床亚组分 后改善带来新思路。此外,通过系列体外功能实
析在内的多层次统计分析,证明:①与癌旁组织相 验,本研究初步证明 B4GALT5 在促进胰腺癌的增
比,B4GALT5 在胰腺癌组织中高表达,提示后续可 殖、运动与浸润功能中发挥重要作用,初步的体内