Page 12 - 南京医科大学自然版
P. 12
第44卷第11期
·1478 · 南 京 医 科 大 学 学 报 2024年11月
A
Bregma -1.22 mm Bregma -1.58 mm Bregma -1.94 mm Bregma -2.30 mm Bregma -2.66 mm
WT
Bmi⁃1 +/-
B 1.2 WT +/- C 1.2 WT +/- D 1.2 WT +/- *
Bmi⁃1
Bmi⁃1
Bmi⁃1
The whole parenchymal (relative to WT) 0.8 * Gray matter volume (relative to WT) 0.8 ** Gray matter volume/ whole DG region (relative to WT) 0.8
1.0
1.0
1.0
0.6
0.6
0.6
0.4
0.4
0.4
volume
0.2
0 0.2 0 volume 0.2 0
HP CA1 DG HP CA1 DG HP CA1 DG
+/-
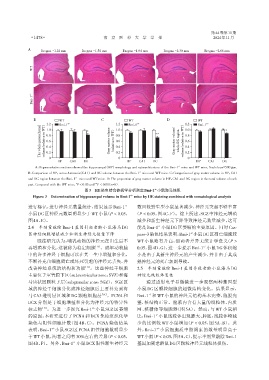
A:Representative sections showed the hippocampal(HP)morphology and cytoarchitecture of the Bmi⁃1 mice and WT mice. Scale bars=500 μm.
+/-
B:Comparison of HP,cornu Ammonis(CA1)and DG volume between the Bmi⁃1 mice and WT mice. C:Comparison of gray matter volume in HP,CA1
and DG region between the Bmi⁃1 +/- mice and WT mice. D:The proportion of gray matter volume in HP,CA1 and DG region in the total volume of each
*
**
part. Compared with the WT mice,P < 0.05 and P < 0.01(n=6).
+/-
图3 HE染色结合体视学分析测定Bmi⁃1 小鼠海马体积
Figure 3 Determination of hippocampal volume in Bmi⁃1 mice by HE staining combined with somatological analysis
+/-
进行标记,进行神经元数量统计,结果显示 Bmi⁃1 +/- 数目较野生型小鼠显著减少,神经元突起不够丰富
小鼠DG区神经元数量明显少于WT小鼠(P < 0.05, (P < 0.05,图4C、F)。综上所述,SGZ中神经元增殖
图4A、E)。 减少和新生神经元下降导致神经元数量减少,这可
+/-
2.4 半剂量敲除 Bmi⁃1 基因引起老龄小鼠海马 DG 能是Bmi⁃1 小鼠DG区萎缩的主要原因。同时Cas⁃
区神经细胞增殖减少和新生神经元数量下降 pase⁃3染色结果表明,Bmi⁃1 小鼠DG区凋亡细胞较
+/⁃
既往研究认为,哺乳动物的神经元在出生后不 WT 小鼠略有升高,但两者差异无统计学意义(P >
再增殖和分化,这被称为稳定细胞 [12] 。成年动物脑 0.05,图4D、G),进一步提示Bmi⁃1 小鼠DG体积缩
+/-
中的许多神经干细胞可以在其一生中增殖和分化, 小是由于其新生神经元的产生减少,并非由于其成
不断补充由细胞凋亡或坏死引起的神经元丢失,并 熟神经元的死亡加剧导致。
改善神经系统的结构和功能 [13] 。这些神经干细胞 2.5 半剂量敲除 Bmi⁃1 基因导致老龄小鼠海马 DG
主要位于室管膜下区(subventricular zone,SVZ)和海 神经元线粒体变性
马齿状回颗粒下层(subgranular zone,SGZ)。SGZ区 通过透射电子显微镜进一步观察两种基因型
域的神经干细胞分化成神经细胞后主要补充到海 小鼠 DG 区颗粒细胞的超微结构变化。结果显示,
马 CA3 透明层区域和 DG 颗粒细胞层 [14] 。PCNA 和 Bmi⁃1 和 WT 小鼠的神经元结构基本完整,胞膜完
+/-
DCX 分别是干细胞增殖和分化为神经元的特异性 整,核结构正常。胞浆内含有大量的线粒体、内质
标志物 [15] 。为进一步探究 Bmi⁃1 小鼠 SGZ 区萎缩 网、核糖体等细胞器(图 5A)。然而,与 WT 小鼠相
+/-
的原因,本研究进行了 PCNA 和 DCX 免疫组织化学 比,Bmi⁃1 小鼠线粒体出现膨大、肿胀,线粒体嵴减
+/-
染色与阳性细胞计数(图 4B、C)。PCNA 染色结果 少的比例较 WT 小鼠增加(P < 0.05,图 5A、B)。此
表明,Bmi⁃1 小鼠 SGZ 区 PCNA 阳性细胞数明显少 外,Bmi⁃1 小鼠细胞质中脂褐素的数量明显高于
+/-
+/-
于WT小鼠,两者之间有30%左右的差异(P < 0.05, WT小鼠(P < 0.05,图5A、C),提示半剂量敲除Bmi⁃1
图4B、F)。另外,Bmi⁃1 小鼠DCX阳性新生神经元 基因加剧老龄鼠DG区颗粒神经元线粒体损伤。
+/-