Page 92 - 南京医科大学自然版
P. 92
第44卷第4期
·530 · 南 京 医 科 大 学 学 报 2024年4月
Glc
GLUT1
Tumor Cell
Glc HBP PGM3 UPR
HK2
MMP⁃3 RRM1
ALDOB FR054
G⁃6⁃P
ROS
G6PD
F⁃6⁃P PPP RPIA
SLC38A5 GSH
PFK
mTOR
F⁃1,6⁃BP ROS
KRAS AMPK
AKT Drug
P⁃Oxid
3⁃PGA Resistance
EGFR PI3K RAF HIF⁃1α
PEP
PKM2
MAPK ERK
Pyr acetyl CoA
PDH
cGAS STING
Lactate PDHK1
Pi
LDHA
MCT4/MCT1 CD147
Lactate
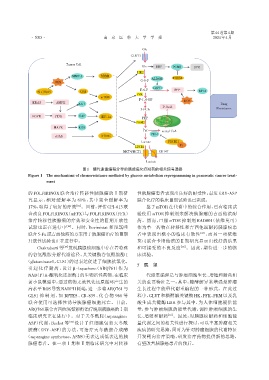
图1 糖代谢重编程介导的胰腺癌化疗耐药的相关信号通路
Figure 1 The mechanisms of chemoresistance mediated by glucose metabolism reprogramming in pancreatic cancer treat⁃
ment
的 FOLFIRINOX 联合治疗转移性胰腺癌的Ⅰ期研 性胰腺癌患者表现出良好的耐受性,最近ERY⁃ASP
究显示,相对缓解率为 61%,其中完全缓解率为 联合化疗的临床Ⅲ期试验也已完成。
17%,取得了较好的疗效 [82] 。目前,评估 CPI⁃613 联 鉴于 mTOR 在代谢中的综合作用,已有临床试
合改良FOLFIRINOX(mFFX)与FOLFIRINOX(FFX) 验使用 mTOR 抑制剂来解决胰腺癌的吉西他滨耐
治疗转移性胰腺癌的疗效和安全性的Ⅲ期开放性 药。然而,口服 mTOR 抑制剂 RAD001(依维莫司)
试验也正在进行中 [83] 。同时,Devimistat 和羟氯喹 作为单一药物在转移性和吉西他滨耐药胰腺癌患
联合5⁃Fu或吉西他滨的方案用于胰腺癌治疗的Ⅲ期 者中表现出极小的临床有效性 [85] ,而另一项依维
开放性试验也正在进行中。 莫司联合卡培他滨的Ⅱ期研究显示出较好的结果
Chakrabarti等 [84] 发现胰腺癌细胞中存在着特殊 和可接受的不良反应 [86] 。因此,期待进一步的临
的谷氨酰胺分解代谢途径,其关键酶谷氨酰胺酶 1 床试验。
(glutaminase1,GLS1)的过表达促进了细胞抗氧化,
5 展 望
引起化疗耐药,设计β⁃lapachone(ARQ761)作为
NAD(P)H⁃醌氧化还原酶1的生物活性药物,在临床 代谢重编程是与肿瘤细胞生长、增殖和耐药相
前小鼠模型中,通过药物无效氧化还原循环产生的 关的重要特征之一,其中,糖酵解异常增强是肿瘤
高水平ROS导致NADPH耗竭,进一步将ARQ761与 生长过程中能量代谢重编程的一种形式。在此过
GLS1 抑 制 剂 ,如 BPTES、CB⁃839、化 合 物 968 等 程中,GLUT 和糖酵解关键酶 HK、PFK、PKM 以及乳
联合使用可选择性诱导胰腺癌细胞死亡。目前, 酸生成关键酶 LDH 参与其中,为人体细胞提供能
ARQ761联合吉西他滨/紫杉醇治疗晚期胰腺癌的Ⅰ期 量,参与肿瘤细胞的能量代谢,调控肿瘤细胞的生
临床研究正在进行中。对于天冬酰胺(asparagine, 长、增殖和耐药 [87] 。因此,对胰腺癌耐药和细胞能
ASP)代谢,Bachet 等 [84] 设计了红细胞包裹天冬酰 量代谢之间的相关性进行探讨,可以丰富肿瘤相关
胺酶(ERY⁃ASP)的方法,可治疗天冬酰胺合成酶 疾病的研究思路,同时为针对肿瘤细胞的代谢特征
(asparagine synthetase,ASNS)无表达或低表达的胰 开发靶向治疗策略、研发治疗药物提供新的思路,
腺癌患者。在一项Ⅰ期和Ⅱ期临床研究中对转移 有望改善胰腺癌患者的预后。