Page 56 - 南京医科大学自然版
P. 56
第45卷第10期
·1424 · 南 京 医 科 大 学 学 报 2025年10月
A Hoechst BODIPY Merge
NC
20 μm 20 μm 20 μm
Stambpl1
20 μm 20 μm 20 μm
B 20 ** C 100 * NC
Bodipy fluorescence intensity 15 5 (mg/g protein) 80 Stambpl1
60
10
40
0
NC Stambpl1 Triglyceride 20 0 Control OA
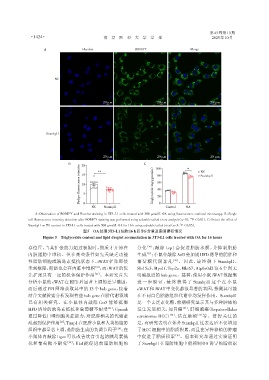
A:Observation of BODIPY and Hoechst staining in 3T3⁃L1 cells treated with 300 μmol/L OA using fluorescence confocal microscopy. B:Single
**
cell fluorescence intensity detection after BODIPY staining was performed using a double tailed t⁃test analysis(n=10,P < 0.01). C:Detect the effect of
*
Stambpl1 on TG content in 3T3⁃L1 cells treated with 300 μmol/L OA for 16 h using a double tailed t⁃test(n=3,P < 0.05).
图5 OA处理3T3⁃L1细胞16 h后TG含量及脂滴累积情况
Figure 5 Triglyceride content and lipid droplet accumulation in 3T3⁃L1 cells treated with OA for 16 hours
存位置,当其扩张能力超过极限时,脂质才开始在 分化 [30] ;敲除 Lcp1 会促进脂肪水解,并抑制脂肪
内脏脂肪中堆积。但在某些条件如先天缺乏功能 生成 [31] ;小鼠中敲除Atf3会加剧HFD诱导的肥胖和
性脂肪细胞或胰岛素抵抗状态下,iWAT 扩张即使 葡萄糖代谢紊乱 [32] 。因此,最终剩下 Stambpl1、
未到极限,脂肪也会在内脏中堆积 [24] ,而iWAT的优 Slc15a3、Myo1f、Top2a、Mki67、Atp6v0d2 这 6 个尚无
先扩张具有一定的机体保护作用 [25] 。本研究首先 明确报道的hub gene。接着,使用小鼠iWAT数据集
分析小鼠的eWAT 在HFD 后显著上调的差异基因, 进 一 步 验 证 ,最 终 获 得 了 Stambpl1 这 个 在 小 鼠
而后通过 PPI 网络获取其中的 13 个 hub gene,接着 eWAT和iWAT中变化都很显著的基因,推测其可能
结合文献检索分析发现有些hub gene在脂代谢领域 在不同白色脂肪组织代谢中均发挥作用。Stambpl1
已有相关研究。在小鼠体内敲除 Ccr5 能够抵御 是一个去泛素化酶,前期研究显示其与多种肿瘤的
HFD 诱导的胰岛素抵抗和葡萄糖不耐受 [26] ;Gpnmb 发生发展相关,如胃癌 [33] 、肝细胞癌(hepatocellular
[34]
通过降低巨噬细胞炎症能力,对肥胖相关的代谢紊 carcinoma,HCC) 、结直肠癌 [35] 等。值得关注的
[27]
乱起到保护作用 ;Timp1在肥胖小鼠和人类的脂肪 是,有研究表明在体外 Stambpl1 过表达后不仅增加
组织中都显著上调,是脂肪生成的负调节因子 [28] ;在 了HCC细胞中的脂质积累,而且在异种移植的肿瘤
小鼠体内敲除 Itgax 可以改善饮食引起的胰岛素抵 中促进了脂质积累 [36] 。但本研究却通过实验证明
抗和葡萄糖不耐受 [29] ;Ubd 能促进前脂肪细胞的 了Stambpl1在脂肪细胞中能抑制OA 诱导的脂质累