Page 132 - 南京医科大学学报自然科学版
P. 132
第43卷第7期
·1018 · 南 京 医 科 大 学 学 报 2023年7月
在与 CRPS 相关的肌张力障碍中起着特殊的作用,
中枢敏化 有待进一步研究。
扣带回
丘脑 ·痛觉过敏 2.2 外周机制
杏仁核 ·异位疼痛 2.2.1 神经炎症
脑干
P物质 CRPS 伴随神经源性炎症增加 。神经源性炎
[9]
谷氨酸
其他机制 症主要由降钙素基因相关肽(calcitonin gene related
痛觉神经 交感神经 ·自身免疫 peptide,CGRP)、P 物质和神经激肽 A 等神经肽介
·遗传因素 导,这些神经肽由 C 纤维末梢通过轴突反射机制释
·心理因素
放。CGRP 激活平滑肌和内皮细胞中的 CGRP1 受
体,诱导小动脉血管化;P物质和神经激肽A通过激
白细胞渗出 活内皮细胞中神经激肽A1受体促进血管通透性;这
组织充血水肿
初始组织损伤 些机制导致充血、组织水肿和白细胞渗出。CGRP
神经损伤 神经源性炎症 和 P 物质不仅可以激活驻留细胞(如肥大细胞和树
突状细胞)释放组胺、血清素、肿瘤坏死因子(tumor
necrosis factor,TNF)⁃α等炎症介质吸引炎症细胞进
NE 一步促进炎症,也作用于局部伤害性Aδ纤维诱导周
CGRP 前列腺素 围神经敏化 [10] 。此外,CGRP 还可以促进汗腺功能
P物质 缓激肽
5⁃羟色胺 和毛发生长 。
[11]
神经激肽A
组胺
2.2.2 自主神经系统紊乱
肥大细胞 中性粒细胞 巨噬细胞
CRPS 患者自主神经系统失衡常导致皮肤颜色
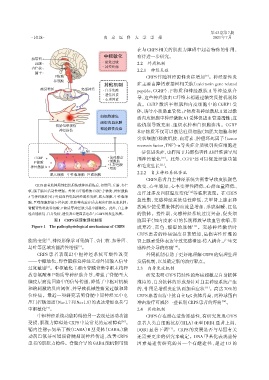
CRPS患者肢体局部组织损伤或神经损伤后,扣带回、丘脑、杏仁 改变、心率增加、心率变异性降低、心排血量降低、
核、脑干脑区活动性增强。外周C纤维释放CGRP、P物质、神经激肽 [12]
出汗过多及四肢温度变化 等临床表现。在 CRPS
A等神经肽作用于外周血管引起神经源性炎症,肥大细胞、中性粒细
急性期,交感神经系统活性降低,去甲肾上腺素释
胞、巨噬细胞释放5⁃羟色胺、组胺等炎症介质表现出组织充血水肿;
脊髓背角释放谷氨酸、P物质等神经肽引起中枢敏化。此外,自主神 放减少使受累肢体的血流量增加,形成温暖、红色
经功能紊乱、自身免疫、遗传及心理因素也参与CRPS的发生发展。 的肢体。慢性期,交感神经系统过度兴奋,促炎细
图1 CRPS病理生理机制图 胞因子(如内皮素⁃1)的长期释放导致血管收缩,形
Figure 1 The pathophysiological mechanisms of CRPS 成寒冷、蓝色、潮湿的肢体 [13] 。交感神经激活时
CRPS 患者的疼痛强度显著增加,是伤害性纤维的
[5]
能的变化 ,神经影像学可见脑干、杏仁核、扣带回、 肾上腺素受体表达导致交感神经⁃传入耦合,产生交
[5]
岛叶等区域功能活性增强 。 感神经介导的疼痛 。
[14]
CRPS 患者表现出中枢神经系统可塑性改变 外周机制有助于更好地理解CRPS的病理生理
——中枢敏化,即脊髓痛觉神经元对外周输入信号 发病机制,以及确定新的治疗靶点。
过度敏感 。中枢敏化主要由脊髓背角中枢末梢释 2.3 自身免疫机制
[6]
放谷氨酸和 P 物质等神经肽介导,增强了脊髓至大 研究表明CRPS持续性的疼痛超敏是自身抗体
脑皮层痛觉回路中的信号传递,降低了中枢对机械 维持的,自身抗体的形成是针对自主神经系统产生
和热刺激的反应阈值,并导致机械性痛觉过敏和异 的,作用是增强炎症从而加重症状 [15] 。高达70%的
位疼痛。最近一项研究表明脊髓中间神经元中电 CRPS患者血清中抗自主IgG抗体升高,丙种球蛋白
[16]
压门控钠通道(Nav1.7和Nav1.8)的表达增加也参与 冲击治疗可减轻一些长期CRPS患者的疼痛 。
[7]
中枢敏化 。 2.4 其他机制
中枢神经系统功能障碍的另一表现是运动功能 CRPS 存在潜在遗传易感性,有研究发现 CRPS
[8]
受损,肌张力障碍是 CRPS 中最常见的运动障碍 。 患者人类白细胞抗原(HLA)亚型 DRB1 显著上调,
鞘内注射γ⁃氨基丁酸(GABA)B 型受体(GABAB )激 DQB1 显著下调 [17] 。CRPS 的发展是否与基因有关
动剂巴氯芬可增强脊髓抑制神经传递,改善 CRPS 还需要更多的研究来确定。DNA 甲基化表观遗传
患者的肌张力障碍。脊髓介导的GABA能机制可能 因素是遗传研究的另一个有趣途径,超过 1/3 的