Page 49 - 《南京医科大学学报(自然科学版)》2026年第3期
P. 49
第46卷第3期 焦 艺,赵廷昱,刘凌翔. 胸腺上皮肿瘤免疫治疗进展与不良事件管理[J].
2026年3月 南京医科大学学报(自然科学版),2026,46(3):355-365,374 ·357 ·
+
+
选择后的 CD4 SP 细胞和 CD8 SP T 细胞会上调 CC type 7,CCR7)的表达,从而促使它们分别向髓质胸
趋 化 因 子 受 体 4(C ⁃ C chemokine receptor type 4, 腺上皮细胞(medullary thymic epithelial cell,mTEC)
CCR4)和CC趋化因子受体7(C⁃C chemokine receptor 上的相关配体迁移,并进入髓质 [22-23] 。
Cortex Clonal deletion Medulla
Negative
Treg selection
cTEC
Bim
FOXP3 IL⁃2
CD25
MHC⁃Ⅱ
MHC⁃Ⅰ
CD4
CD8
TCR
DP DP
CD28
No/Strong interaction CD80/86
interaction
Moderate
Positive
selection AIRE FEZF2
DC
TRA TRA
mTEC
Apoptosis CD8 SP Cross presentation of TRAs
+
+
CD4 SP
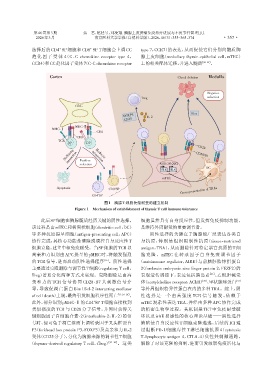
图1 胸腺T细胞免疫耐受的建立机制
Figure 1 Mechanism of establishment of thymic T cell immune tolerance
此后SP细胞在胸腺髓质经历关键的阴性选择, 细胞虽然具有自身反应性,但发挥免疫抑制功能,
该过程是由mTEC和树突状细胞(dendritic cell,DC) 是维持外周耐受的重要调节者。
等多种抗原提呈细胞(antigen⁃presenting cell,APC) 阴性选择的关键在于胸腺能广泛表达各类自
协作完成,其核心功能是清除或调控自身反应性 T 身抗原,特别是组织限制性抗原(tissue⁃restricted
细胞克隆,建立中枢免疫耐受。当SP细胞的TCR以 antigen,TRA),从而删除针对特定器官抗原的 T 细
高亲和力识别由 APC 提呈的 pMHC 时,将触发强烈 胞克隆。mTEC 在转录因子自身免疫调节因子
的TCR信号,进而启动阴性选择程序 [16] 。阴性选择 (autoimmune regulator,AIRE)与前脑胚胎锌指蛋白
主要通过克隆删除与调节性T细胞(regulatory T cell, 2(forebrain embryonic zinc finger protein 2,FEZF2)的
Treg)谱系分化两种方式来实现。克隆删除是由高 表观遗传调控下,表达包括胰岛素 [31] 、乙酰胆碱受
[32]
亲和力的 TCR 信号协同 CD28⁃B7 共刺激信号介 体(acetylcholine receptor,AChR) 、甲状腺球蛋白 [33]
导,导致促凋亡蛋白 Bim(Bcl⁃2 interacting mediator 等外周组织特异性蛋白在内的多种TRA。综上,阴
of cell death)上调,最终引发细胞程序性死亡 [17,24-26] 。 性选择是一个由高强度 TCR 信号触发、依赖于
此外,部分识别pMHC⁃Ⅱ的CD4 SP T细胞在接收到 mTEC 混杂性表达 TRA、并经由多种 APC 协作完成
+
类似强度的 TCR 与 CD28 分子信号,并同时获得关 的精密生物学过程。其机制是 TET 中免疫耐受破
键细胞因子白细胞介素⁃2(interleukin⁃2,IL⁃2)的信 坏以及 irAE 易感性的核心理论基础——阴性选择
号时,便可免于凋亡继而上调转录因子叉头框蛋白 缺陷使自身反应性 T 细胞克隆逃逸,后续的 ICI 通
P3(forkhead box protein P3,FOXP3)及高亲和力IL⁃2 过阻断 PD⁃1/细胞毒性 T 淋巴细胞抗原 4(cytotoxic
受体(CD25分子),分化为胸腺来源的调节性T细胞 T⁃lymphocyte antigen 4,CTLA⁃4)负性共刺激通路,
(thymus⁃derived regulatory T cell,tTreg) 。这类 解除了对该克隆的抑制,进而引发级联免疫活化与
[27- 30]