Page 101 - 南京医科大学自然版
P. 101
第44卷第5期 李盈盈,冯黎黎,韩 峰. 胶质母细胞瘤对替莫唑胺耐药机制的研究进展[J].
2024年5月 南京医科大学学报(自然科学版),2024,44(5):688-697 ·689 ·
为5⁃(3⁃甲基三氮烯⁃1⁃)咪唑⁃4⁃酰胺[5⁃(3⁃methyltri⁃ 第7位氮原子以及鸟嘌呤第6位氧原子上。甲基化
azen⁃1⁃yl)imidazole⁃4⁃carboxamide,MTIC],MTIC 进 的腺嘌呤和鸟嘌呤在 DNA 复制过程中形成错误配
一步分解成甲基重氮阳离子和甲基肼 [10] 。其中,甲 对,引起单链和双链 DNA 断裂,细胞周期被阻滞在
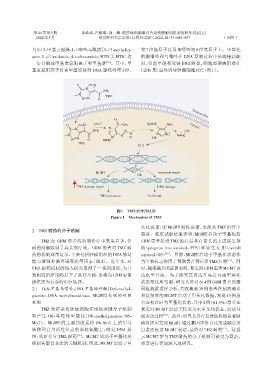
基重氮阳离子将其甲基转移到 DNA 腺嘌呤第3位、 G2/M 期,最终诱导肿瘤细胞死亡(图1)。
O N
N
NH2
N
TMZ
N N O
O Exetracellur
O N pH>7 NH2 H2NOC NH2 Cytosol
N N
NH2 N CH3
N N N N NH N N
N H AIC
N
N O MTIC
TMZ +
CH 3
MGMT G mismatch repair
CH3
DNA damage repair DNA damage
TMZ resistance Cell death
图1 TMZ的作用机制
Figure 1 Mechanism of TMZ
基化患者,即 MGMT 阴性患者,更能从 TMZ 治疗中
2 TMZ耐药的分子机制
获益。临床试验结果表明,MGMT 启动子甲基化的
TMZ 在 GBM 患者的初期治疗中效果显著,但 GBM 患者接受 TMZ 治疗后具有更长的无进展生存
耐药问题限制了其长期疗效。GBM 患者对 TMZ 耐 期(progress free survival,PFS)和总生存期(overall
药的机制异常复杂,主要包括肿瘤组织的DNA修复 survival,OS) 。目前,MGMT启动子甲基化状态作
[11]
能力增强和微环境变化等因素(图 2)。近年来,对 为生物标志物用于预测患者预后及TMZ疗效 。同
[12]
TMZ 耐药机制的深入研究取得了一系列进展,为开 时,越来越多的证据表明,复发的GBM患者MGMT表
发相应治疗策略打下了良好基础,也将为GBM患者 达水平升高。为了探究其表达升高是否由甲基化
提供更为有益的治疗选择。 状态变化所引起,研究人员对614例GBM患者的基
2.1 O⁃6⁃甲基鸟嘌呤⁃DNA甲基转移酶(O⁃6⁃methyl⁃ 因组数据进行分析,共收集到38例患者在初次确诊
guanine⁃DNA methyltransferase,MGMT)关联的耐药 和复发时的MGMT启动子甲基化数据,发现13例患
机制 者在初诊时为甲基化状态,其中8例(61.5%)患者在
TMZ 发挥杀伤肿瘤细胞作用的关键分子机制 复发时MGMT 启动子转变为未甲基化状态,启动基
[13]
即产生 O6⁃鸟嘌呤甲基化(O6⁃methylguanine,O6⁃ 因表达过程 。此外,研究人员在复发胶质瘤患者肿
MeG)。MGMT 的主要功能是将 O6⁃MeG 上的甲基 瘤组织中发现MGMT通过基因重排方式形成融合蛋
转移到自身活性位点的半胱氨酸上,修复 DNA 损 白进而促进MGMT表达,最终对TMZ耐药 。这提
[11]
伤,从而介导 TMZ 耐药 [10] 。MGMT 启动子甲基化是 示MGMT参与TMZ耐药的分子机制可能更为复杂,
抑制其蛋白表达的关键机制,因此,MGMT启动子甲 需要进行更加深入地研究。