Page 102 - 南京医科大学自然版
P. 102
第44卷第5期
·690 · 南 京 医 科 大 学 学 报 2024年5月
MGMT Metabolic reprogramming
MGMT GST
CCL2 Glycolysis (O2)
DNA damage
…
O6⁃MeG AA,steroid PUFA,FASN
CH3
Dislipidemia
CH3
DNA damage TMZ resistance
DNA damage repair Glioma stem cell
Mismatch repair
NHEJ CH3
TMZ
HRR MGMT
ATP⁃binding cassette transporter
GBM
Abnormal signal pathways Tumor microenvironment
Pericyte
Bcl⁃2 familly Anti⁃apotosis Endothelial cell
Vessel CCL5⁃CCR5
PI3K/AKT signal pathways
Wnt/β⁃catenin signal pathways Endothelial cell
EMT
Others TMZ resistance DNA damage repair
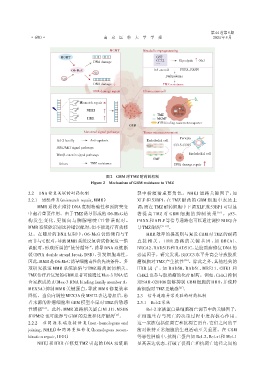
图2 GBM对TMZ耐药的机制
Figure 2 Mechanism of GBM resistance to TMZ
2.2 DNA修复关联的耐药机制 裂中扮演着重要角色。NHEJ 通路关键因子,如
2.2.1 错配修复(mismatch repair,MMR) XLF 和 53BP1,在 TMZ 耐药的 GBM 细胞中表达上
MMR系统在维持DNA复制精确性和预防突变 调;而在 TMZ耐药细胞中下调XLF或53BP1可以显
中起着重要作用。由于TMZ诱导形成的 O6⁃MeG结 著 提 高 TMZ 对 GBM 细 胞 的 抑 制 效 果 [16] 。 p53、
构发生变化,更倾向与胸腺嘧啶(T)错误配对。 PAXX和APLF等信号通路也可以通过调控NHEJ介
MMR系统能识别这种错误配对,但不能进行有效修 导TMZ耐药 [17-19] 。
复。在随后的 DNA 复制中,O6⁃MeG 仍然倾向与 T HRR效率的提高则与复发GBM对TMZ的耐药
而非与C配对,导致MMR系统反复尝试修复这一错 直 接 相 关 。 HRR 通 路 的 关 键 基 因 ,如 BRCA1、
误配对,形成所谓的“徒劳循环”,诱导 DNA 双链断 BRCA2、RAD51B和RAD51C,是胶质瘤修复DNA的
裂(DNA double strand break,DSB),引发细胞毒性。 必需因子。研究发现,BRCC3水平升高会导致胶质
因此,MMR是O6⁃MeG诱导细胞毒性的先决条件。多 瘤细胞对TMZ产生抗性 [20] 。除此之外,其他经典的
项研究报道 MMR 系统缺陷与 TMZ 耐药密切相关。 HRR 因 子 ,如 RAD50、RAD51、MRE11、CHK1 和
TMZ治疗后复发的GBM患者可能通过Mex⁃3 RNA结 CHK2也参与胶质瘤的化疗耐药。例如,CHK1抑制
合家族成员A(Mex⁃3 RNA binding family member A, 剂 SAR⁃020106 能够抑制 GBM 细胞的 HRR,并使肿
MEX3A)抑制 MMR 关键蛋白,导致 MMR 修复效率 瘤细胞对TMZ更敏感 。
[21]
降低。当负向调控MEX3A使MSH2表达增加后,患 2.3 信号通路异常关联的耐药机制
者来源的肿瘤细胞和 GBM 模型小鼠对 TMZ 的敏感 2.3.1 Bcl⁃2家族
性增强 [14] 。此外,MMR 通路相关蛋白 MLH1、MSH6 Bcl⁃2 家族蛋白是细胞凋亡调节中的关键因子,
[15]
和PMS2 也可能参与GBM的复发和化疗耐药 。 在细胞生存与死亡的决策过程中发挥核心作用。
2.2.2 非同源末端连接修复(non⁃homologous end 这一家族包括促凋亡和抗凋亡蛋白,它们之间的平
joining,NHEJ)和同源重组修复(homologous recom⁃ 衡对维持正常细胞的生理活动至关重要。在 GBM
bination repair,HRR) 等恶性肿瘤中,抗凋亡蛋白如 Bcl⁃2、Bcl⁃xl和 Mcl⁃1
NHEJ 和 HRR 在修复 TMZ 引起的 DNA 双链断 呈高表达状态,打破了促凋亡和抗凋亡途径之间的