Page 73 - 南京医科大学自然版
P. 73
第45卷第10期 王 勇,丁 磊,董汇昱,等. APOE对前列腺癌细胞增殖、迁移和侵袭的影响[J].
2025年10月 南京医科大学学报(自然科学版),2025,45(10):1435-1442,1512 ·1441 ·
A *
0.5
*
si⁃NC *
(mg) 0.4
0.3
Tumor weight 0.2
si⁃APOE
0.1
si⁃APOE+ARi
0
si⁃NC si⁃APOE si⁃APOE+ARi
B
1 500
si⁃NC
***
si⁃APOE
(mm 3 ) 1 000 *** *** si⁃APOE+ARi
Tumor volume 500
0
3 6 9 12 15 18 21 24 27 30
Time(d)
***
*
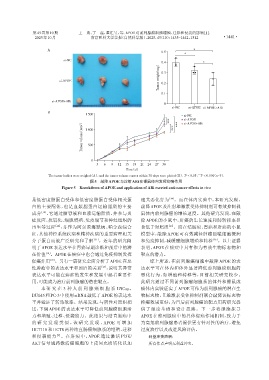
The tumor bodies were weighed(A),and the tumor volume curves within 30 days were plotted(B). P < 0.05, P < 0.001(n=3).
图5 敲降APOE与注射ARi在裸鼠体内发挥抑癌作用
Figure 5 Knockdown of APOE and application of ARi exerted anti⁃cancer effects in vivo
是低密度脂蛋白受体和低密度脂蛋白受体相关蛋 速其恶化行为 [24] 。而在体内实验中,本研究发现,
白的主要配体,也是血浆脂蛋白运输脂质的主要 敲降APOE及注射雄激素受体抑制剂可有效抑制裸
成分 [19] ,它通过脑脊液和血浆运输脂质,并参与炎 鼠体内前列腺癌的增长速度。其他研究发现,在敲
症反应、抗氧化、细胞增殖、免疫调节和神经组织的 除 APOE 的小鼠中,肝癌的生长速度和肺转移率显
再生等过程 [20] ,并作为阿尔茨海默病、帕金森综合 著低于对照组 [25] 。而在结肠癌、胃癌和肝癌的小鼠
征、其他神经系统疾病和精神疾病的重要病理相关 模型中,敲除 APOE 可有效减轻肿瘤巨噬细胞浸润
分子蛋白而被广泛研究和了解 [21] 。近年的研究阐 和免疫抑制,减缓癌细胞增殖和转移 [26] 。以上证据
明了APOE表达水平在胃癌早期诊断和预后中的潜 表明,APOE 在癌症中具有作为有效生物标志物和
在价值 [10] 。APOE在癌症中也会通过免疫抑制发挥 靶点的潜力。
促癌作用 [22] 。另有一篇研究全面分析了APOE 在恶 综上所述,在前列腺癌细胞中敲降 APOE 的表
性肿瘤中的表达水平和预后的关系 [23] ,说明其异常 达水平可在体内和体外显著降低前列腺癌细胞的
表达水平可能在癌症的发生和发展中起着重要作 恶化行为,如增殖和转移等,目前相关研究较少。
用,可能成为治疗前列腺癌的潜在靶点。 此研究通过不同前列腺癌细胞系的体外和裸鼠成
本 研 究 在 3 种 人 前 列 腺 癌 细 胞 系 LNCap、 瘤体内实验证实了APOE可作为前列腺癌的潜在生
DU145和PC⁃3中使用siRNA敲低了APOE的表达水 物标志物,且雄激素受体抑制剂联合敲降该标志物
平并验证了转染效率。结果发现,与阴性对照组相 抑癌效果更好,为日后前列腺癌的靶点用药研究提
比,下调 APOE 的表达水平可降低前列腺癌细胞活 供了理论基础和设计思路。下一步将继续探寻
力和增殖、迁移、侵袭能力。此结果与结直肠癌中 APOE 在前列腺癌中的具体促癌作用机制,致力于
的 研 究 发 现 类 似 ,该 研 究 发 现 ,APOE 可 增 加 为高危前列腺癌患者提供更有针对性的治疗,避免
HCT116和HCT8两种结直肠癌细胞系的增殖、迁移 过度治疗以及改进风险评估。
[9]
和侵袭能力 。在肝癌中,APOE 通过激活 PI3K/ 利益冲突声明:
AKT 信号通路激活癌细胞的上皮间充质转化以加 所有作者声明无利益冲突。