Page 13 - 南京医科大学自然版
P. 13
第45卷第11期 戴欣媛,夏 天,朱 磊,等. RNA结合蛋白RBMS3通过稳定p21 mRNA抑制乳腺癌增殖[J].
2025年11月 南京医科大学学报(自然科学版),2025,45(11):1537-1545,1571 ·1543 ·
p21 mRNA 3′⁃UTR的ARE,提高其稳定性。 接结合p21 mRNA 3′⁃UTR 的ARE,增强其稳定性并
2.4 敲低 p21 可逆转 RBMS3 过表达诱导的乳腺癌 上调 p21 表达,进而抑制乳腺癌细胞增殖的分子机
细胞增殖抑制 制。这一发现为RBMS3的抑癌功能提供了新视角,
为验证 RBMS3 诱导的乳腺癌细胞增殖抑制是 丰富了转录后调控网络在乳腺癌中的作用认知。
否依赖于 p21,将敲低 p21 的 siRNA(Si⁃p21)或对照 RBMS3在卵巢癌、肺癌、胶质母细胞瘤、乳腺癌和
siRNA(Ctrl)转染至 RBMS3 过表达细胞。qRT⁃PCR 肝细胞癌等多种肿瘤中被证实为抑癌因子 [7,11,14-16] ,但
与 WB 检测显示,Si⁃p21 可有效敲低 p21 的 RNA(图 既往有研究提出“三阴性乳腺癌中外源性表达
5A、B)与蛋白水平(图 5C~F)。集落形成实验显示, RBMS3 不影响细胞增殖”的观点 [12] 。既往研究中
敲低p21可部分挽救RBMS3过表达引起的细胞增殖 RBMS3功能存在的争议,可能源于以下方面:其一,
抑制(图5G~J);EdU实验结果与之一致(图5K~N)。 细胞模型差异:永生化乳腺上皮细胞无法完全模拟
表明 RBMS3 通过上调 p21 抑制乳腺癌细胞增殖。 恶性乳腺癌细胞的增殖调控特性;其二,检测方法
敏感性:单一磺酸罗丹明 B 检测的局限性可能掩盖
3 讨 论
增殖表型,而本研究通过EdU掺入、集落形成、细胞
本研究首次揭示 RNA 结合蛋白 RBMS3 通过直 周期、凋亡和异种移植瘤模型等多维度实验,均证
A B C
SUM⁃1315⁃NC SUM⁃1315⁃SCR MDA⁃MB⁃231⁃NC
mRNA (%) 100 SUM⁃1315⁃RBMS3 * (%) 100 SUM⁃1315⁃shRBMS3 mRNA (%) 100 MDA⁃MB⁃231⁃RBMS3
*
*
75
Relative p21 remaining 50 T1/2>8 h Relative p21 mRNA remaining 50 * * * T1/2=4.0 h Relative p21 remaining 50 * T1/2=4.2 h
75
75
*
*
T1/2=4 h
25
T1/2=2.1 h
25
25
T1/2=1.9 h
0
0 2 4 6 8 0 0 2 4 6 8 0 0 2 4 6 8
Time after Act D Time after Act D Time after Act D
treatment(h) treatment(h) treatment(h)
D E F G
MDA⁃MB⁃231⁃SCR SUM⁃1315 *** MDA⁃MB⁃231
mRNA (%) 100 MDA⁃MB⁃231⁃shRBMS3 p21 Input IgG RBMS3 -200 bp (%) 150 p21 Input IgG RBMS3 -200 bp
100
75
Relative p21 remaining 50 * * * T1/2=2.2 h β⁃actin -300 bp Relative expression of mRNA p21 50 β⁃actin -300 bp
25
0
0 2 4 6 8 T1/2=1.2 h 0 lgG RBMS3
Time after Act D
treatment(h)
H I J K
ARE 2.0 NC * 2.0 NC *
Relative expression of (%) mRNA p21 50 Mutant probe p21 3′⁃UTP Relative luciferance assay 1.5 Relative luciferance assay 1.5
RBMS3
RBMS3
150
***
100
1.0
1.0
ARE
0.5
0.5
0
IgG RBMS3
U to G 0 PGL3 p21 3′⁃UTP mutant ARE 0 PGL3 p21 3′⁃UTP mutant ARE
SUM⁃1315 MDA⁃MB⁃231
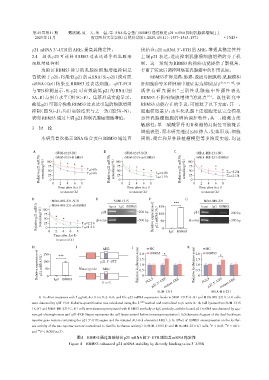
A-D:After treatment with 5 μg/mL Act D for 0,2,4,6,and 8 h,p21 mRNA expression levels in SUM⁃1315(A,B)and MDA⁃MB⁃231(C,D)cells
were detected by qRT⁃PCR. Relative quantification was calculated using the 2 -ΔΔCt method and normalized to β⁃actin. E-H:Cell lysates from SUM⁃1315
(E,F)and MDA⁃MB⁃231(G,H)cells were immunoprecipitated with RBMS3 antibody or IgG antibody,and the bound p21 mRNA was detected by aga⁃
rose gel electrophoresis and qRT⁃PCR(Input represents the cell lysate control before immunoprecipitation). I:Schematic diagram of the dual⁃luciferase
reporter gene vectors containing the p21 3'⁃UTR region and the mutated AU⁃rich elements(ARE). J,K:Effect of RBMS3 overexpression on the lucifer⁃
ase activity of the two reporter vectors(normalized to Renilla luciferase activity)in SUM⁃1315(J)and MDA⁃MB⁃231(K)cells. P < 0.05,P < 0.01,
**
*
and *** P < 0.001(n=3).
图4 RBMS3通过直接结合p21 mRNA的3′⁃UTR增加其mRNA稳定性
Figure 4 RBMS3 enhanced p21 mRNA stability by directly binding to its 3′⁃UTR